Соли аммония
В начале урока можно провести опрос, для того чтобы обобщить уже известный учащимся материал о соединениях азота; повторить сведения о происхождении (генезисе) иона аммония и механизме его образования; выявить признаки сходства между аммиаком и ионом аммония пo составу и строению, взаимосвязь между ними. Два ученика выполняют у доски следующие задания: 1. Запишите уравнения химических реакций, при которых образуется ион аммония, и схему механизма образования этого иона. 2. Сравните состав и строение аммиака я иона аммония; определите, возможно ли наличие у них общих свойств (окислителя или восстановителя).
Пока учащиеся готовятся к ответу, учитель проводит фронтальный опрос: сколько электронов образует внешний электронный слой атома азота?
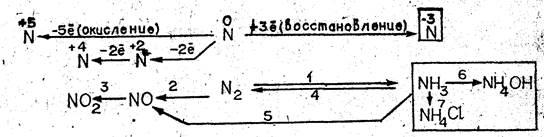
Какие предельные степени окисления азота вам известны? Назовите промежуточные степени окисления азота 1. На основе ответов учащихся учитель записывает на доске схему взаимосвязи соединений азота, а ниже — другую схему, соответствующую первой, используя формулы соединений азота и отражая в ней свойства уже изученных веществ. Порядок записи показывают номера над стрелками в схеме (см. рис. 1).
Затем учитель предлагает следующим двум учащимся записать уравнения реакций, соответствующие превращениям 1—3 и 4, 5, отметив условия их протекания и рассмотрев как окислительно-восстановительные процессы (превращения 6, 7 будут описаны первым учеником, вызванным к доске).
Из ответов первых двух учащихся следуют выводы: 1. Катион аммония образуется при соединении молекулы аммиака с протоном молекулы кислоты; новая ковалентная связь возникает, по донорно-акцепторному механизму. 2. Аммиак и ион аммония имеют одинаковый качественный и близкий количественный состав, следовательно, между ними возможна взаимосвязь; азот в этих соединениях имеет степень окисления —3, значит, они могут проявить только восстановительные свойства.
Из записей на доске учитель оставляет те, которые относятся к генезису и строению иона аммония, а также правую часть схемы превращений и продолжает беседу. Учащиеся прогнозируют состав соединений, содержащих катион аммония, и приводят в качестве примера гидроксид и соли аммония. На доске записываются тема урока и формулы галогенидов, сульфата, нитрата, карбоната аммония. На основе анализа общей формулы учащиеся прогнозируют проявление у изучаемых соединений общих свойств солей, особенных — характерных только для солей аммония (причина — наличие катиона. NH) и единичных (индивидуальных), свойств, отсутствующих у других солей. Эти свойства обусловлены сочетанием иона аммония с определенным анионом.
Учащиеся прогнозируют сходство в свойствах солей калия и аммония, указывают на ионный характер кристаллической решетки, хорошую растворимость солей в воде. Рассмотрение образцов солей подтверждает выводы. Необходимо подчеркнуть различие: соли аммония, имеют сложный катион, состоящий из двух элементов, поэтому кроме сходных свойств должны быть и отличительные.
По заданию учителя учащиеся перечисляют общие свойства солей: 1) соли — электролиты, в водных растворах диссоциируют на ионы; 2) для солей характерны реакции обмена, идущие в направлении образования практически нерастворимых соединений, газов, малодиссоциирующих веществ. Если ученики назову» третье общее свойство — способность к гидролизу, можно позднее кратко рассмотреть; его особенности и выявить отличие солей аммония от солей калия.
Учащиеся записывают уравнения реакций электролитической диссоциации, отмечают наличие одинакового катиона (NH) — причину общности свойств солей аммония. Затем она называют варианты реакций обмена: соль кислота, соль — соль, соль — щелочь. Приводя конкретные примеры для реакций первого варианта, учащиеся учитывают, что сильная кислота вытесняет слабую из соли, а практически нелетучая, летучую. Учитель может продемонстрировать опыт взаимодействия твердого хлорида аммония с концентрированной серной кислотой. Записывая уравнение реакции, отмечаем, что ион аммония сохраняется, следовательно, эта реакция не является характерной именно для солей аммония.
Другое о образовании:
Система работы по развитию театрализованных игр с перчаточными
куклами у детей 6 года жизни
На основе данных, полученных на констатирующем этапе, был составлен проект "Театр бибабо и дети" Задачи проекта: Создать условия для активной творческой деятельности старших дошкольников, участвующих в театрализованной деятельности. Создать условия для совместной театрализованной деятельн ...
Использование игр при обучении иностранному языку
Применение игры для развития навыков иноязычной речи – еще недостаточно изученная область педагогики. Не всякая игра (пусть самая живая и интересная) подходит для этой цели. Поэтому выбор нужной игры – одна из первых задач преподавателя иностранного языка. Этот выбор должен проводиться с учетом цел ...
Методика работы по формированию фонематического восприятия и речевого слуха
у дошкольников
Бесспорна взаимосвязь развития фонематического восприятия не только с фонетической, но и с лексико грамматической стороной речи. При планомерной работе по развитию фонематического слуха дошкольники намного лучше воспринимают и различают окончания слов, приставки, общие суффиксы, выделяют предлоги в ...

